PermaPro® – die synthetische Alternative
PermaPro – hochdichte PTFE-Barrieremembran
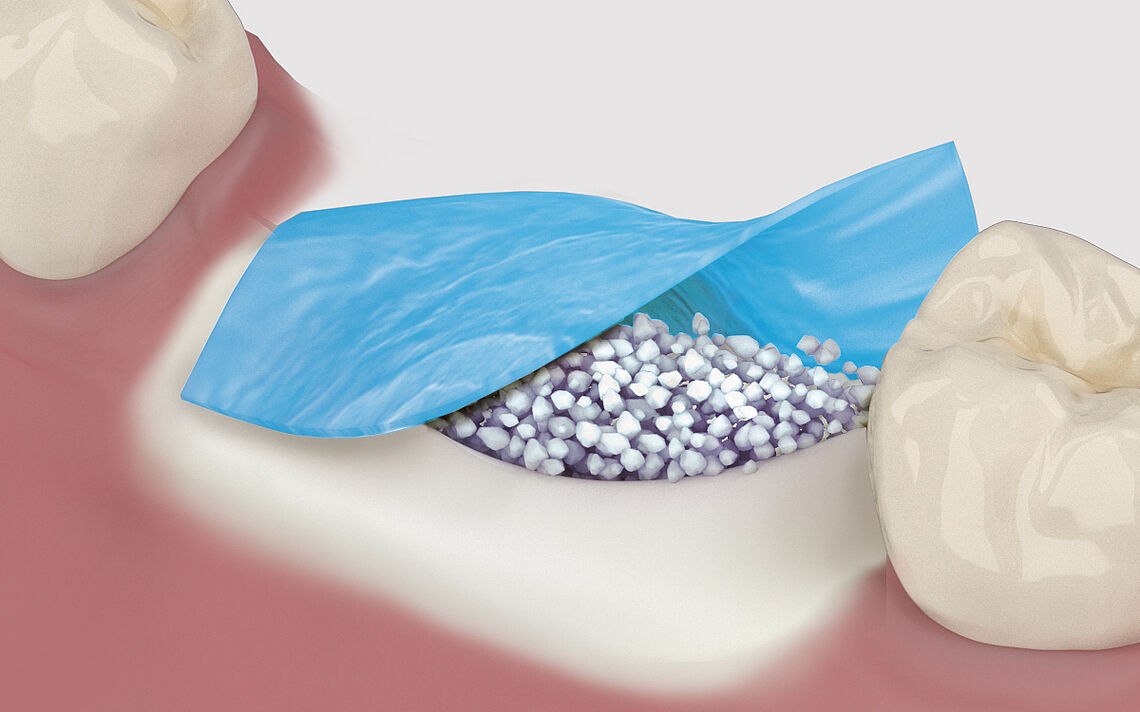
PermaPro ist eine außergewöhnlich dünne, nicht resorbierbare, biologisch inerte und biokompatible Membran, die aus hochdichtem Polytetrafluorethylen (PTFE) hergestellt wird. Die PermaPro Membran behält ihre strukturellen Eigenschaften – sowohl bei der initialen Implantation als auch während der gesamten Einheilungszeit. Aufgrund ihrer dichten Struktur wirkt die Membran als effiziente Barriere gegen bakterielle und zelluläre Penetration, daher kann sie bei bestimmten Verfahren nach Indikationsstellung offen einheilen.
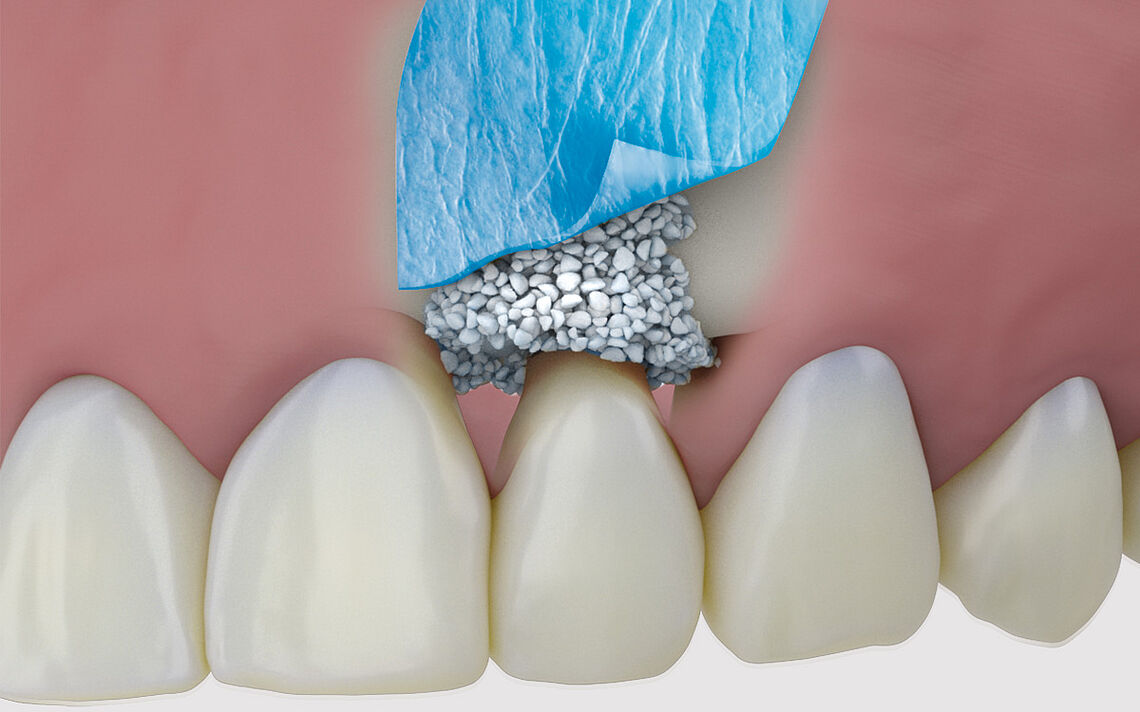
Die Anwendung von PermaPro wird vor allem für die Regeneration knöcherner Defekte außerhalb der Kammkontur empfohlen, da die Membran im Vergleich zu resorbierbaren (Kollagen-)Membranen eine höhere Stabilität und hinsichtlich Raumerhaltung überlegene Eigenschaften hat. Darüber hinaus ermöglicht die offene Einheilung mit PermaPro bei der Socket- und Ridgepreservation, dass die Weichgewebearchitektur und -kontur erhalten bleibt, da kein primärer Wundverschluss erforderlich ist. Dadurch wird eine koronale Verschiebung der Mukogingivalgrenze vermieden und die anhaftende/keratinisierte Gingiva bleibt erhalten.
Eigenschaften der PermaPro
- Höhere Formstabilität gegenüber handelsüblichen Kollagenmembranen
- Augmentation außerhalb der Kieferkammkontur
- Synthetisches Material – keine religiösen oder ernährungsbezogenen Konflikte
- Offene Einheilung, Exposition – Situationen, in denen ein primärer Wundverschluss nicht gewünscht ist (indikationsabhängig)
PermaPro – synthetische, nicht resorbierbare PTFE-Membran
- 100 % synthetische PTFE-Barrieremembran
- Ultradünn (ca. 0.08 mm)
- Aufgrund der dichten Struktur undurchlässig für Bakterien Einfach zu entfernen – wegen des nur geringen Einwachsens von Gewebe in die Oberflächenstruktur
- Kein primärer Wund-/Weichgewebeverschluss erforderlich (indikationsabhängig)1,2
- Einfaches Wiederauffinden dank der blauen Farbe
- Abgerundete Kanten minimieren ein Gewebetrauma
- Einfache Befestigung mit Nähten oder Fixationspins
Regeneration und Augmentation
Ziel jeder Geweberegenerationstechnik, und insbesondere der Knochentransplantation, ist es, die Bildung von lebendem und reaktivem Gewebe zu erreichen, das in der Lage ist, sich nachhaltig umzubauen, um die mechanische und biologische Funktion langfristig zu erhalten. Wenn das native Knochenvolumen für die Insertion von Implantaten unzureichend ist, sind häufig Maßnahmen zum Aufbau des Alveolarknochens erforderlich.
Die Augmentation kann beispielsweise nach Knochenabbau, Parodontalerkrankung, Zahnextraktion oder Trauma – abhängig von der Indikationsstellung – vor oder simultan zur Implantation erfolgen.
PermaPro – synthetische, nicht resorbierbare PTFE-Membran
PermaPro ist eine temporäre Barrieremembran, die eine hohe Formstabilität und einen guten Volumenerhalt aufweist. Sie findet Ihre Anwendung in der GBR bei mehrwandigen ausgedehnten vertikalen Kieferkammdefekten.
- Alveolen- und Kieferkammerhalt (offene Einheilung)
- Horizontale/vertikale Kammaugmentation
- Fenestrations- und Dehiszenzdefekte
- Intraossäre Defekte (1- bis 3-wandig)